
Back سيتوكروم 3A4 Arabic CYP3A4 English CYP3A4 Esperanto CYP3A4 Spanish Tsütokroom P450 3A4 Estonian CYP3A4 Persian CYP3A4 Finnish CYP3A4 French Taurochenodeossicolato 6alfa-idrossilasi Italian CYP3A4 Japanese
| Cytochrom P450 3A4 | ||
|---|---|---|
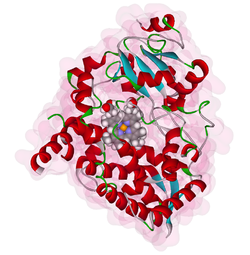
| ||
| Strukturmodell von Cytochrom P450 3A4 mit zentraler Hämgruppe nach PDB 1W0E | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 503 AS; 57,3 kDa | |
| Kofaktor | Häm | |
| Bezeichner | ||
| Gen-Name | CYP3A4 | |
| Externe IDs | ||
| Enzymklassifikationen | ||
| EC, Kategorie | 1.14.13.32, Monooxygenase | |
| Reaktionsart | Oxidation | |
| Substrat | Albendazol + NADPH/H+ + O2 | |
| Produkte | Albendazol-S-oxid + NADP+ + H2O | |
| EC, Kategorie | 1.14.13.67, Monooxygenase | |
| Reaktionsart | Hydroxylierung | |
| Substrat | Chinin + NADPH/H+ + O2 | |
| Produkte | 3-Hydroxychinin + NADP+ + H2O | |
| EC, Kategorie | 1.14.13.97, Monooxygenase | |
| Reaktionsart | Hydroxylierung | |
| Substrat | Lithocholat + NADPH/H+ + O2 | |
| Produkte | Hyocholat + NADP+ + H2O | |
| Vorkommen | ||
| Übergeordnetes Taxon | Wirbeltiere | |
Cytochrom P450 3A4 (abgekürzt: CYP 3A4) ist ein Isoenzym der Cytochrom P450-Superfamilie. Es ist im menschlichen Körper einer der zentralen Bestandteile der Verstoffwechselung (Biotransformation) insbesondere körperfremder Stoffe (Xenobiotika). Cytochrom P450 3A4 kommt mengenmäßig am meisten in der Leber vor. Es hat die meisten Substrate aller Cytochrome. Da auch viele Arzneistoffe über Cytochrom P450 3A4 abgebaut werden, ist es das Zentrum vieler Arzneimittelinteraktionen. Es ist das am meisten gebildete Cytochrom P450 und verstoffwechselt etwa die Hälfte aller Arzneistoffe.[1]
- ↑ F. P. Guengerich: Cytochrome P-450 3A4: regulation and role in drug metabolism. In: Annual review of pharmacology and toxicology, 1999, Band 39, S. 1–17, doi:10.1146/annurev.pharmtox.39.1.1, PMID 10331074.